
英语原文共 46 页,剩余内容已隐藏,支付完成后下载完整资料
烯酮衍生物的立体控制转化获得立体化学丰富的天然产物的启发结构
Taleb H. Al-Tel,* Vunnam Srinivasulu, Mani Ramanathan, Nelson C. Soares, Anusha Sebastian, Maria L. Bolognesi, Imad A. Abu-Yousef和Amin Majdalawieh
a沙迦大学沙迦医学研究所,邮箱27272,沙迦,阿联酋
b美国大学生物、化学和环境科学系沙迦、沙迦、阿联酋
c母校药学与生物技术学系- Universitagrave; di博洛尼亚,贝梅洛罗路,6,40126博洛尼亚,意大利
摘要:近二十年来,人们对复杂自然产物和受自然启发的分子的设计艺术进行了大量的研究。在这几十年里,大量的合成成果,特别是以多样性为导向的合成(DOS),实现了立体控制、步经济和原子经济合成原理的基本见解。这增强了合成设计中三维视觉的可视性,并通过将今天的多样性导向合成(DOS)置于前沿位置,从而实现了对具有高度立体化学和骨骼复杂性的各种支架的访问,从而实现了戏剧性的增长。为此,开始基于材料的方法是DOS中使用的强大工具之一,允许快速访问高sp3含量的分子结构。骨骼和立体化学多样性往往是最重要的选择性调制的生物功能互补蛋白在生物空间。在这种背景下,环己二烯酮支架的立体控制转化,已经将自己定位为一个强大的平台,以快速生成丰富的立体化学和天然产物为灵感的化合物集合。本文综述了利用环己二烯酮衍生物作为多能构件,构建新型化学空间的多向合成策略。
- 介绍
随着DOS的使用,化学家对合成艺术的定义发生了变化。这也许是亨德里克森在1975年描述得最好的,当时他将“理想合成”描述为一种具有正确定位功能的复杂分子结构。这份由Hendrickson撰写的概念报告,在原子和步经济反应的概念被正式激活之前,就真正理解并代表了当今综合设计的“经济”。今天,DOS领域,特别是构建/配对/配对——以及基于材料的初始方法,已经达到了一个显著的水平许多人宣称合成已经成熟。但是,也许在得出这一结论之前,人们需要反思一下大自然是怎样令人振奋地创造其最复杂的分子的(例如,具有264个立体异构体的孢毒素),然后才能宣告合成的科学已经完全成熟。如此惊人的自然复杂性对化学学会来说是一个巨大的挑战,他们要努力创新合成方法,可能是受到了自然创造力的启发。为此,天然产物具有丰富的结构和立体化学多样性,然而,在药物发现活动中使用它们存在许多障碍。这可能是由于它们用于筛查和临床试验的数量有限。1-3因此,在过去10年左右,利用面向多样性的合成(DOS)策略的特权和受自然启发的脚手架的重新构建得到了极大的增强。在这些策略中,4-6是构建/配对/配对和初始材料为基础的策略。这些策略利用多能构件的多向转化,构建了具有高3d含量的立体化学多样性结构。7-9许多报告表明,高sp3含量的化合物文库是非常理想的,因为越来越多的科学界相信,在一个特定文库中更多的sp3中心可以增强对生物大分子靶标的选择性和效力。此外,许多最近的报告指出,增加sp3-在临床环境中,化合物收集中的含量降低了毒性和化合物消耗率。11,12也就是说,环己二烯酮衍生物在过去十年左右已经成为一个强大的平台,允许进入复杂的体系结构。通常情况下,这些分子是受自然启发和/或具有生物学吸引力的分子。13-16在这篇综述中,我们的目标是强调2,5-环己二烯酮影响的立体控制策略,并说明其强大的通用性作为一种工具,用于建造特权和受自然启发的建筑。
1.1 面向多样化综合的关键战略
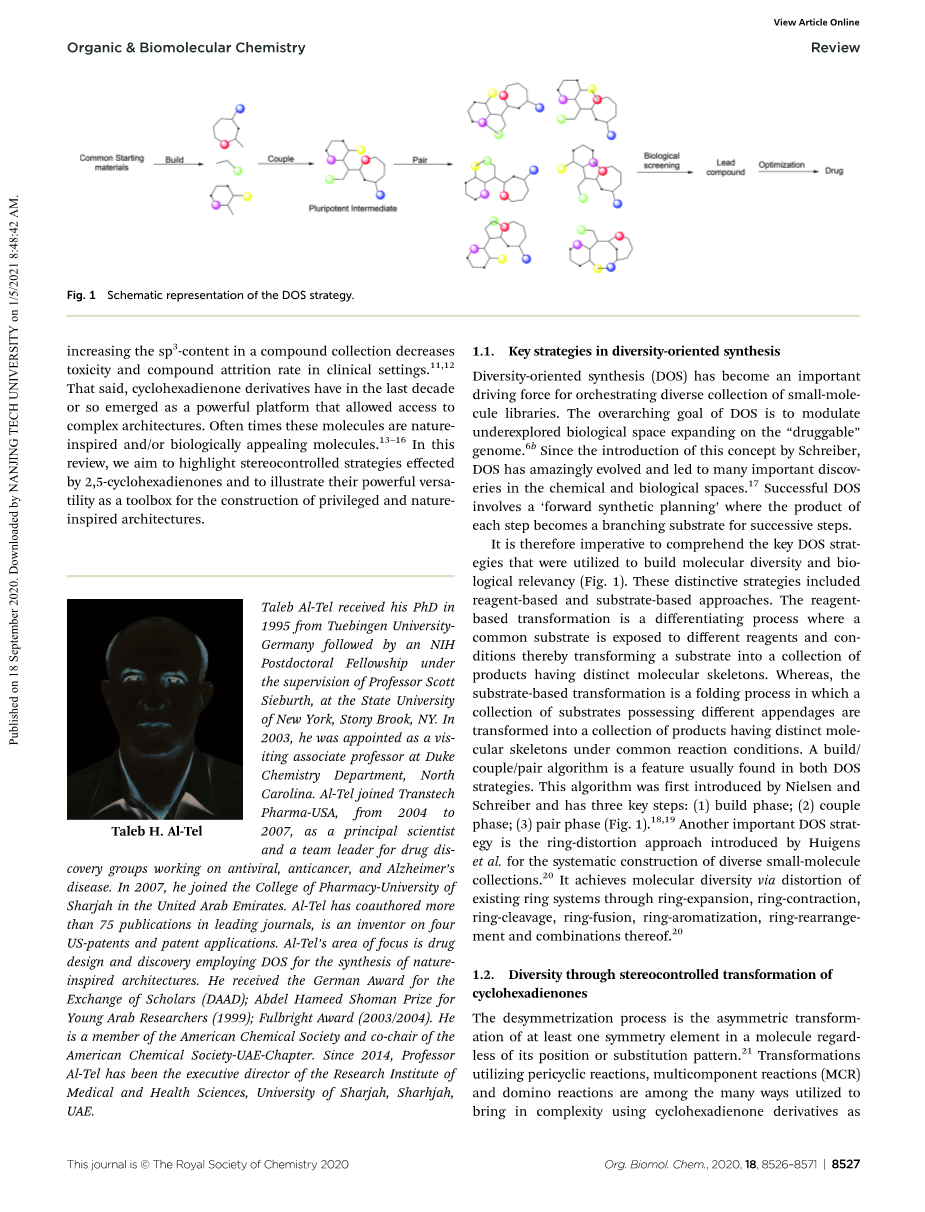
面向多样性的合成(DOS)已经成为协调小分子库的多样化集合的重要驱动力。DOS的首要目标是调节未充分探索的生物空间,并扩大“可用药”基因组。自从Schreiber引入这个概念以来,DOS已经令人惊讶地发展,并导致了许多化学和生物空间的重要发现。成功的DOS包括“前向综合规划”,即每一步的产物成为后续步骤的分支基板。
因此,有必要了解用于构建分子多样性和生物学相关性的关键DOS策略(图1)。这些独特的策略包括基于试剂和基于底物的方法。基于试剂的转化是一种分化过程,其中一个共同的基质暴露在不同的试剂和条件下,从而将基质转化为具有不同分子骨架的产物集合。而基于底物的转化是一种折叠过程,将具有不同附属物的一组底物利用共同的反应条件转化为具有不同分子骨架的一组产物。构建/配对/配对算法是两种DOS策略中常见的特性。该算法首先由Nielsen和Schreiber提出,有三个关键步骤:1)构建阶段;2)几个阶段;3)配对阶段(图1)。18,19 另一个重要的DOS策略是Huigens等人为系统构建多样化小分子集合而引入的环畸变方法。它通过环扩张、环收缩、环裂、环融合、环芳构化、环重排及其组合来扭曲现有的环系统,从而跟踪分子多样性。
图1 DOS策略的原理图表示
1.2 环己二烯酮立体控制转化的多样性
不对称化过程是指分子中至少一个对称元素的不对称变换,而不考虑其位置或取代方式。21利用周环反应、多组分反应(MCR)和多米诺反应的转化,是利用环己二烯酮衍生物作为起始材料带来复杂性的多种方法之一。22,23在合成与对映体富集的环己酮有关的复杂天然产物类似物的各种方法中,环己二烯的催化去对称法被用作最有效的方法之一。Incarviditone, ( )- rishiilide B和(-)-cepharatine D是为数不多的由2,5-环己二烯酮衍生物的多样性定向反对称反应获得复杂天然产物的例子。24-27由于环己二烯酮衍生物含有多种反应性官能团,这些官能团被实现了多种手性支架的立体控制转化(图2)。
图2.2,5-环己二烯酮的多面反应性研究
1999年,Feringa等人展示了第一个通过有机锌试剂共轭加成取代环己二烯酮的不对称不对称反应的例子。这份报告为研究人员以化疗和区域选择性的方式利用这些构建模块铺平了道路。这篇综述综述了过去十年报道的各种优势多样性导向平台,这些平台可以生成适合于2,5-环己二烯酮衍生物的生物活性的截取天然产物。交付的产品基于如图3所示的三个主要环己二烯酮构建块组织成两个主要架构。
O
O
O
R1 R2
R1 哦
R1 NHR2
RO或者O N H
O H
H O
刺桐碱核
何
MeO
N我MeO
(-) -mesembrine
H H N H
N( )-亚胺嘧啶OH H H
R X n maalioxide类似物
我我
H
H
H Me Me CO2H我
retigeranic酸啊
H
哦,家
吗啡的核心
O
哦啊
H
H O
H HO H rach -incarvilleatone .(法语
O H H O H
O O
H HO O
H rac-incarviditone
O
MeO何
H MeO O azicemycin A和B核心
N
CF3
N
CF3 Incargranine B模拟
N NMe
O
(-) -strychnopivotine啊我
我
在N终极战士
H O Me O Me ( )- isoplendine
看我的脸色
O (R S *, *, *) oic模拟
我N
哦
H N
啊,啊,马达加斯加山诺尔
图3,DOS库生成使用2,5-环己二烯酮
2. 2,5-环己二烯系烯烃的非对映选择性转化
有两套基质属于这一类;末端为烯烃的2,5-环己二烯酮另一个内部有烯烃基。受这些底物影响的立体控制反应将在以下几节中讨论。
2.1. 5,6/ 6,6-双环支架的合成
Rauhut-Currier (RC)反应也被称为vinylogous Morita-Baylis-Hillman反应,代表了一种形成碳-碳键的高效合成方法,能够高度选择性地构建复杂框架。29 .几个研究小组已广泛利用2,5-环己二烯酮与末端烯基的RC反应的分子内应用。例如,Sasai等人在2012年开发了一种原子经济、非对映体和对映选择性的方法,利用多功能化手性氨基膦催化分子内RC策略,以优异的收率构建具有医学意义的alpha;-烷基烯-gamma;-丁内酯。遵循一种概念上类似的策略,黄的实验室开发了一种多功能手性氨基膦催化的不对称分子内Rauhut-Currier (AIRC)反应,该反应以环己二烯酮为底物。该方案生成了一系列具有四元中心的氢- 2h -吲哚,具有良好的非对映选择性(gt;20:1 d.r and gt;99% ee;方案1)。最初,二苯基膦基在丙烯酸酯单元上发生Michael加成,得到烯酸膦基I。在烯酸I和其中一个烯烃之间又发生Michael加成,得到中间产物II。随后的质子转移过程导致手性氢- 2h -吲哚(含氮吲哚)(2)以及催化剂的再生(方案2)。合成电位通过将氢- 2h -吲哚转化为高度功能化的产物(4和6;方案1)。
方案1通过分子内Rauhut-Currier序列进行对映选择性转化
Ph2P
O
O
O
O
N
R Ts
2 b
Ts
R
N
O
1 b
O
O
N
H
Ph2P
H
O O
O
2
PPh2
O N Ts
R
N Ts
N H
O O H
我
R
方案2 提出的AIRC进程机制。
Lu和他的同事扩展了这些发现,开发了一种高效的手性胺(beta;-ICD)催化分子内RC程序,用于获得具有出色的过剩对映体的双环alpha;-丙烯-gamma;-丁内酯(8)(方案3)。32采用外消旋的gamma;-取代的2,5-环己二烯酮烯丙烯酸酯作为前体,通过RC反应实现了前所未有的对偶烯平行动力学拆分(DKR),从而导致手性对偶烯(8a)的对映富集。如图4所示,烯丙酸部分的存在为进一步的结构操纵提供了机会。在同一组的另一篇报告中,具有垂链烯酮部分(11)的环己二烯酮被转化为具有光学富集的双环吡喃(13)和海蛇丹(12)骨架。33这种转变的一个显著特征是硫脲和烯酮部分的羰基氧之间的氢键相互作用,从而将原本灵活的中间体(III)锁定在有利的位置,以促进所需的环化过程(方案4)。
方案3 烯炳酸酯分子内的对映选择性rc型合成。
方案4 悬臂烯酮的对映选择性合成(11)。
2018年,Chegondi实验室披露Rh-catalyzed arylative环合的enone-tethered cyclohexadienones通过串联共轭加成(方案5)。通过芳基化反应所得的拴在enone和顺向水解Rh-enolate其次是基地的介导环合导致cis-fused二环enones(19)具有优良的选择性很大。顺式熔合双环产品承载烯酮功能是有价值的合成手柄。其中一种用于制备这些支架的方法是在脱硅条件下合成一种三环酮衍生物来传递化合物(20)。机械地,beta;-氢化物从rh烯醇(VII)的消除使用水(方案6)。
方案5.顺式融合双环烯酮的双共轭加成非对映选择性合成。
方案6.rh催化环己二烯酮衍生物芳基功能化的建议。
涉及烯丙基亲核试剂的催化对映选择性1,4加成反应仍然不发达。围林等人调查手性phosphinooxazoline-nickel催化拆分desymmetrization allenyl 2,与arylboronic 5-cyclohexadienones酸生成cis-fused hexahydroindol-5-one或与三个连续的立体高hexahydrobenzofuran-5-one diastereo和选择性(方案7)。这种转化是通过芳基硼酸与烯丙基2,5-环己二烯酮分子内的1,4-连
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[259443],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 播撒生物炭促进鸟粪石形成,但加速重金属积累外文翻译资料
- 钢铁工业余热有机朗肯发电的能量及炯分析外文翻译资料
- 深度共晶溶剂微波辅助处理木质素-碳水化合物复合 物的高效裂解及超快提取木质素低聚物外文翻译资料
- 功能化杯状芳烃离子团族[4]的合成、晶体结构及竞争结合性能外文翻译资料
- 面向高能量密度柔性超级电容器的无纺布用黑磷杂化微纤维的微流控纺丝结构外文翻译资料
- 活性炭对水溶液中氨的吸附外文翻译资料
- 制备可控海胆状NiCo2S4微球协同硫掺杂石墨烯作为高性能 二次锌空气电池的双功能催化剂外文翻译资料
- 钛酸盐材料对重金属离子的吸附外文翻译资料
- CO2敏感催化剂的合成与表征温度响应催化聚离子液体微凝胶外文翻译资料
- 温度响应微凝胶薄膜在湿环境中作为可逆二氧化碳吸收剂外文翻译资料


