
英语原文共 7 页,剩余内容已隐藏,支付完成后下载完整资料
京都大学化学研究所(日本)
电双层结构的研究
第一部分:二恶烷对双层容量的影响
由渡边晃,福井Tsu和静冈上田
6个数字在12个细节和1个表
(1963年5月6日收到)
介绍
在以前的通信中,报道了双层结构的研究,该研究使用与碱金属卤化物水溶液接触的滴汞电极(1)进行。 目前的工作是为了通过使用二恶烷水混合物作为溶剂更详细地阐明该结构。 主要问题是检查二氧六环在汞表面上的吸附行为,并且借助于这种行为的浓度依赖性,将水溶液作为二氧杂环己烷零浓度的限制情况处理。
向水溶液中加入二恶烷的效果表征为二恶烷的表面活性和溶剂介电常数的降低。 从定义中可以清楚地看出,“表面活性”对双层扩散部分的结构没有主要影响。 这是由于这部分的性质是由泊松玻尔兹曼方程确定的,该方程基于溶液相的整体性质。 因此,加入二恶烷的效果是以这样的方式改变扩散双层中的介电常数,使得电场增加发生,导致其厚度增加并因此其差分电容降低。
船尾吸附的结构,另一方面,二恶烷的表面活性(如果有的话)以及该层中抗衡离子溶剂化的变化强烈地影响了该层。 众所周知,表面活性材料如辛醇等强烈地吸附在汞电极上,因此在电毛细管最大值附近的极化范围内导致双层电容降低。 但是,这种现象并不局限于所谓的表面活性材料,但也可以以较少的表面活性物质或者甚至在表面不活泼的材料中找到。 就添加材料的介电常数低于水的介电常数而言,由于在小双层电场的极化范围内斯特恩层中存在该物质,所以预计容量降低。
本文在理论和实验上处理了电场对双层中二氧六环分布的影响。 也期望目前的处理适用于许多其他非离子材料,并且还适用于离子材料并稍作修改。
试验
物料
碘化钾,溴化物,氟化物和氯化钠的等级为(Merck),未进一步纯化。 容量数据显示,可能存在于这些材料中的痕量杂质对滴汞电极的容量具有可忽略的影响。 通过用稀水洗涤来纯化汞。 硝酸,然后进行真空蒸馏。 通过离子交换树脂纯化的水用锡冷凝器蒸馏; 这给了特定导电率的水ca. 10-6ohm-1cm-1,其用于所有实验。 二氧六环在钠金属存在下蒸馏两次并保持在O00。 以这种方式新鲜制备的二恶烷没有显示在两周内使用的任何极谱波的醛和其他杂质。
双层容量的测量
汞溶液的不同容量界面通过使用Grahame交流电桥法(2)在30plusmn;0.05°测量。 桥由滴汞电极DME组成,两个非导电标准电阻,每个600欧姆,一个非电感电阻十年Rs总电阻100千欧姆,可以0.1欧姆为单位进行调节,一个云母电容器Cs总电容为11.111微法拉可调以0.0001微法为单位。 C8和R8串联起来作为电桥的等效补偿支路。 由CR产生的12 mV和840 cps的交流电压。
将真空管振荡器施加到桥上,并且使用高增益调谐交流放大器通过阴极射线示波器检测桥平衡。 示波器的水平扫描通过闸流管继电器电路和锯齿波扫描电压发生器与DME同步。 因此,通过正确选择0 8和Rs,oscillo scopic屏幕上的轨迹会聚在水平时间轴上的某个点上,表明当时的桥梁平衡。 液滴的界面面积是由液滴生长速率和会聚点在水平轴上的位置计算的; 在当前的实验中,这一点总是在下降开始增长后的1.8秒时被采用。 然后通过Os值和界面面积计算每单位面积的极化电施加到DME上,通过在电池底部具有大量水银池的电位计作为参考电极。 DME的水银头保持在72.5厘米,产生的滴加速率为0.0007克/秒。 下降的时间是约。 4秒,这取决于极化。 在每次运行之前,通过在溶液中鼓泡纯氢气流来除去氧气。
结果
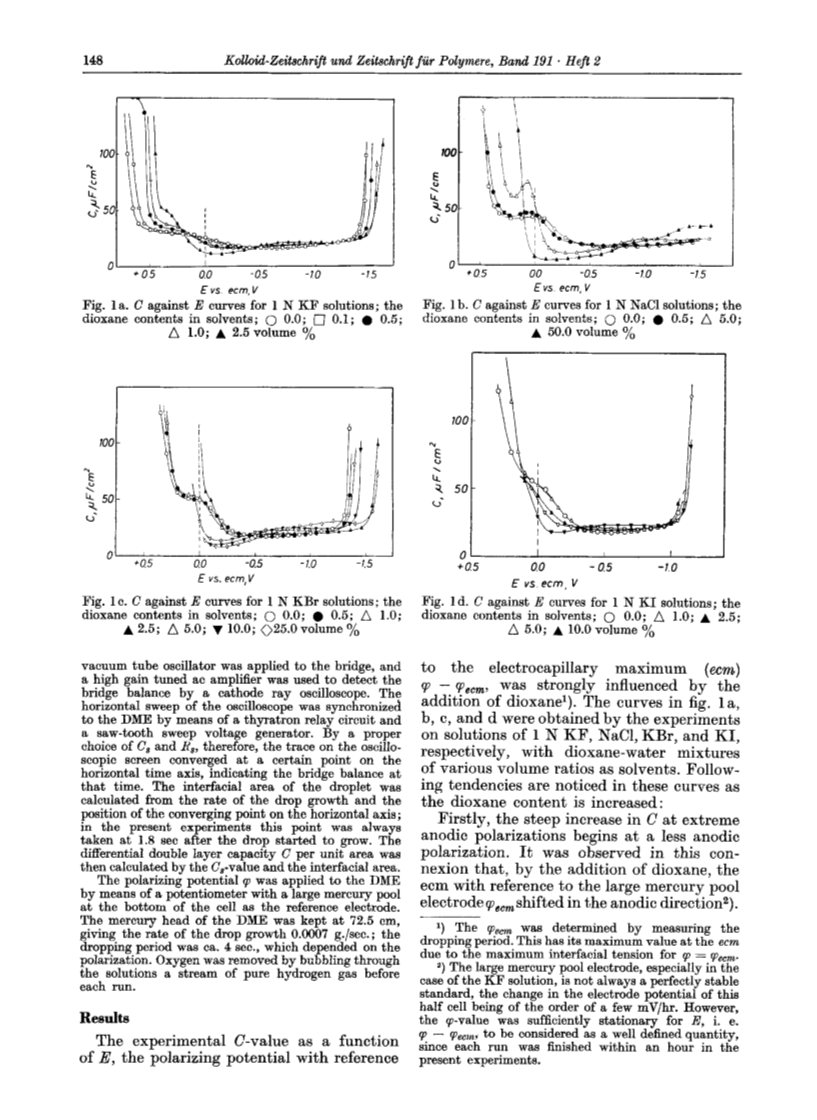
作为E的函数的实验0值,参考极化电位至电毛细管最大(ecm)(fJ - ffJecm,受二恶英添加量1的强烈影响)。 图中的曲线。 通过对各种体积比的二恶烷 - 水混合物作为溶剂,分别用1N KF,NaCl,KBr和KI的溶液进行实验获得1a,b,c和d。 随着二恶烷的含量增加,在这些曲线中注意到趋势:
首先,在极端阳极极化下O的急剧增加始于较小的阳极极化。 在这种关系中观察到,通过添加二氧杂环己烷,ecm参照在汞阳极方向上移动的大汞池电极2)。
1)f / Jeem是通过测量滴期确定的。 这在ecm处具有最大值,这是由于对于lt;p = f / Jecm·的最大界面张力
2)特别是在KF溶液情况下,大型水银电极电极并不总是一个完全稳定的标准,这种电极电位的变化
半电池的数量级为几毫伏/小时。 然而,对于E而言,rp值足够平稳,即rp-f / Jecin,被认为是确定的量,因为在本实验中每个运行在一小时内完成。
其次,在阳极极化下观察到C的增加。 二恶烷的这种作用取决于溶液中的离子种类,氟化物最大,碘化物最小。
最后,容量抑制发生在ecm附近。 这种现象与表面活性剂溶液中观察到的浓度低于完全单层吸附的浓度相似(3)。 二恶烷的吸附也在ecm附近的潜在范围内发生。 然而,由于二恶烷的表面活性小,与用表面活性剂溶液观察到的最小平面相比,最小值相对较尖锐。 这种能力抑制也可以用含有其他有机物质,如邻,间,对二氯苯甲酸,甘氨酸等无机电解质溶液来观察(4)。
汞表面的电荷密度:通过实验的图形积分将q#39;计算为E的函数
C对E曲线(5),即
q#39;= Jc dE
讨论
Gouy漫漫双层:
这层Ca的差分容量
是根据泊松波尔兹曼方程(6)推导出来的。 对于zz价电解质的溶液,以下等式成立(7):
Cc =(z Ae / kT)(1 qc / 4 A2)112, [2]
和
A = De k T n / 2 n。 [3]
这里n是溶液体内每单位体积电解质的分子数; De是该层中的介电常数; qa是从Stern平面延伸到溶液体内的单位横截面溶液柱中的总电荷; k是玻尔兹曼常数; T是绝对温度; e是基本电子收费。 对于在30℃下的一种正常的单价电解质溶液,将出现上述等式:
Ca = 19.14(1.752Da qa2)1 12mu;F/ cm2· [4]
在高双层的影响下,由于电介质饱和,扩散双层中的介电常数几乎总是小于体积值.然而,由于我们目前没有直接测量Da的方法,所以根据大量的介电常数由方程式[4]计算Ca值,其由本文作者用Schering桥在1000处测量cps和30°C。
对于各种二氧六环含量的1N电解质溶液获得的理论Cc对Qa曲线表明Ca是qa的对称函数,在qa = 0时最小。对于较高的二氧杂环己烷含量,最小值较小。 如果在图1中的零偏振范围上C的最大抑制。 1仅仅是由于Ca对Qa曲线的最小值,前者会
在C0与q#39;曲线中不存在,其中C0是斯特恩层能力(9)。
如此获得的C0与q#39;曲线与相应的C对q#39;曲线的比较表明后一组曲线的特征在前一组曲线中被大量地保留。 因此,我们可以得出结论二恶烷的加入完全归因于斯特恩结构的变化(吸附)层。
等式[5]仅在离子不存在特定吸附的情况下才存在,因此当q#39;= qc时,这种假设仅在非常有限的情况下有效,例如KF水溶液(5,10)。 然而,就我们正在处理的电解质含量高的溶液,例如1N溶液,因此具有高Ca值而言,得到的结论,即C对Ca的不敏感性不受此类影响限制。
积分能力:
积分容量K由(5)
K = Q#39;/ E。 [6]
由于在目前的实验条件下,扩散双层的容量对总双层电容的影响可以忽略不计,因此Eis与介电常数D和斯特恩层的有效厚度x有关,方程如下:
K = D / 4nx。 [7]
图1显示了KF解决方案的K对q#39;曲线。 2和其他解决方案与此处观察到的趋势基本相同; 这些是通过使用等式[6]从实验q#39;对E曲线,等式[1]获得的。 在没有二恶烷的情况下,正q#39;的K值总是大于负q#39;的K值。 这可以通过一般阴离子的较大极化率来解释,即方程[7]中较大的D值与阳离子(5)的相比较。 在二恶烷的存在下,发生二氧杂环己烷的吸附,其通过在零电荷区域上的容量抑制来指示。
随着负q#39;的增加,二恶烷的解吸发生并且K接近零二恶烷含量的值。 另一方面,随着积极q#39;的增加,K的增加如此之大以至于K最终超过零二恶烷含量的相应值。 K的增加较大,获得更高的二恶烷含量。 这可以通过阴离子比阳离子更容易脱水来解释。 由于二恶烷的解吸在该极化范围内不完全,因此二恶烷的存在会影响斯特恩层中水分子与阴离子之间的相互作用。 在这一层中二氧六环分子引起的取向水分子的位移有可能帮助阴离子脱水,从而导致方程[7]中x值的减小,其结果是K阳离子的增加另一方面,难以脱水(5),因此随着负q#39;的增加K的增加归因于二氧六环的解吸。
容量抑制理论
二恶烷的加入显着抑制了零极化范围内的K值。 但是,如果这种极化的话,汞电极在负方向上增加,抑制变小,最后达到K值与离子双层相同的阴极电位。 这意味着二氧杂环己烷的解吸由于增加的双层电场而发生,也就是吸附的正静电自由能的增加。 虽然在这种情况下容量行为因阴离子脱水而变得复杂,但阳极极化也会发生同样的情况。
理论处理从计算自由能变化的静电部分i i Qel开始,用于将二氧六环分子从体相中带入斯特恩层中的过程,同时水分子的数量相应减少指向斯特恩图层。 计算方法与电解液盐析效应的Debye方程式(11)相同。 静电场的自由能在离汞的距离x处产生体积元素dV,电荷密度q的表面由下式给出:
0
(DF2/ 8:n :) dV =(q2/ 8:n:Dtimes;4dV,
其中D是介质的介电常数。 这里q是一个虚拟量,定义为一个有效的电荷密度,它与双层场有关,方程为F = -q / Dx2。 这些事会晚一些讨论。经过简单的计算我们就可以得到
下面的等式(12):
一个]
其中nd和nw是每厘米数3,vd和vw分别是二恶烷和水的分子体积。 如果我们假设线性关系,即。
D = Dd N Dw(1-N), [9]
,
方程[8]变成(12):
LJGe-1 y。bull;Vw Dw-Dd [10]
- 8 n xbull; Dw2 #39;
其中Dd和Dw分别是二恶烷和水的二电常数,N是二恶烷的摩尔分数。斯特恩层K(cm-2)的积分能力假定为等于离子双层的积分容量Kw和二氧杂环己烷吸附层Kd的平行组合,因此Kd
K = Kw(1-theta;) Kdtheta;, 0≦theta;≦1, [11]
其中0是二恶烷的覆盖度。 在Langmuir型单层吸附二恶烷的假设下,吸附平衡表示为N的函数:
theta;=bN/(1 bN) [12]
这里b是平衡常数,其中与电化学自由能有关吸附∆G的研究.
∆G= - kTln b。 [13]
由于∆G是静电(LIQel)和化学(LIG)术语的总和,后者代表二氧杂环己烷的特定吸附,我们从方程[10]得到下式:
dG = aq2 ∆G [14]
当 a = ( Vw/8pi;)[(Dw-Dd)/] [15]
将方程[12]代入方程[11],就成了 [16]
当 ∆K=Kw-K [17]
即观察到的积分容量的抑制,以及
∆Kd=Kw-Kd [18]
即 在条件1≦bN下获得的∆K值,即对应于完全二氧杂环己烷单层的最大抑制。
从等式[12],[13]和[14]获得的理论theta;与q曲线在图2中给出。 3用于任意选择的 ∆G / kT和a / kT的值。 每条曲线相对于q = 0轴是对称的,q = 0时最大值。对于较高的∆G / kT,在较低的N值处达到相同的容量抑制∆K。 对于较小的a / kT,随着q绝对值的增加,∆K下降的斜率变小。与实验进行比较
实验∆K与q#39;曲线如图2所示。 4a,b,c和d与二恶烷内容作为参数。 除了一些小的差异之外,曲线的一般形状与图1中的理论曲线非常吻合。 该理论的基本思想是正确的:双层场有助于增加二氧六环的解吸。 可以看出,∆K最大值并不总是出现在q#39;= 0处。但是,一般情况显然倾向是最大的高二恶烷含量在q#39;= 0时出现。由于该位置的偏差和q#39;= 0的最大值始终在负方向,可以通过水偶极子的方向来解释,它们的负极指向汞表面,在ecm处; 必须对汞表面施加额外的负电荷,以使水偶极子的取向随机分布。由于二恶烷分子具有可忽略的小偶极矩(13),因此当二氧六环分子发生水分子置于斯特恩层时,取向效应减弱。 事实上,无花果的直线。 4a,b,c或d连接每组曲线的最大点在坐标∆K = ∆Kd处与轴q#39;= 0相交。 这意味着当完全单层吸附二氧杂环己烷的情况下q#39;= 0时发生最大抑制。
值得注意的是,这条直线在极化处切割横坐标对应于q#39;〜 - 10mu;库尔/厘米2,与
KF的例外(-4mu;库尔/厘米2)。 这导致了重要的结论,即双层场的绝对零点在水溶液中以这个量偏移到负极化。该不对称的该试验相对于轴的∆K对q#39;曲线q= 0是理论和实验之间的另一个差异。 这里%是给出最大L1K的q#39;值。 前面的部分表明,即使对于大的正极化,残留在斯特恩层中的二氧杂环己烷也有助于使阴离子脱水。 随着q#39;的增加,K的增加归因于两种机制,即阴离子特异性吸附和二氧杂环己烷解吸中的增加。 这解释了这样的事实,即∆K对q#39;曲线通常倾斜地
全文共7936字,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[9652],资料为PDF文档或Word文档,PDF文档可免费转换为Word


