
英语原文共 10 页,剩余内容已隐藏,支付完成后下载完整资料
在Cu置换ZSM-5催化剂上通过甲烷和二氧化碳同时共活化直接合成乙酸
摘要:这项研究的最终目标是开发一种新的战略,以更有效和更清洁地开发甲烷和二氧化碳资源。由于甲烷和二氧化碳的高稳定性,甲烷和二氧化碳同时活化碳氢键是催化领域最棘手的挑战之一。利用M -ZSM-5催化剂(M = Li , Na , K 和Ca2 ),在连续流微反应器系统中同时进料甲烷和二氧化碳,催化生成乙酸。在425-525 ℃温度范围内,CO2和CH4共同进料,在360 mL/h的低空速下,以甲烷为基础,观察了乙酸的形成。与Cu0-H-ZSM-5相比,M -ZSM-5催化剂显著提高了乙酸的生成速率,催化效率依次为K gt; Na gt; Ca gt; Li。结果表明, M 以碳酸盐的形式在催化剂表面富集并活CO2,随后与Cu0-H-ZSM-5活性化的碳氢键发生反应。Cu0-H-ZSM-5催化剂聚集了Cu0和M ,在500 ℃稳态下运行10 h,乙酸的生成速率最高(395 mu;mol/(g·cat·h))。
- 介绍
来源丰富且有价值的化学品,如二氧化碳和甲烷等全球变暖气体,不仅从能源和环境问题的角度,而且由于其作为替代和经济原料的潜在用途,引起了人们的极大关注。对于甲烷和二氧化碳的催化转化,使用非均相催化剂的表面活化被认为是克服非常高的热力学和动力学稳定性的可行方法之一。然而,这个反应在热力学角度上是非常不利的(△G0 = 16.98 kcal/mol)。据估计,即使在特殊的实验条件下(725 ℃,100 atm,CO2 (95%)和CH4 (5%),甲烷的热力学平衡转化率也低至1.6times;10-6。此外,虽然同时活化两种分子看起来很有吸引力,但是却更加困难。甲烷的碳氢键活化是在非氧化或氧化条件下,在氧化剂的帮助下,通过催化分解甲烷的碳氢键来实现的。然而,二氧化碳活化被认为需要还原剂来失氧,或者至少应该在金属Lewis酸位点或碱位点的帮助下进行分子活化。
至于乙酸,目前最流行的乙酸生产工艺是甲醇羰基化工艺,该工艺由铑、铱配合物与HI体系组成,分为三个步骤。因此,与当前主要的乙酸方法相比,通过在相同的催化剂体系中同时活化这两种分子,通过甲烷与二氧化碳的羧化一步形成乙酸具有很大的优点,但是由于高热力学障碍,同时活化两种反应物分子非常具有挑战性。首次被报道的在CF3COOH溶剂中钯/铜配合物催化CH4和CO2合成乙酸,其中K2S2O8 (15 mol%)均匀地作为氧化剂,乙酸产率为7%。然而,在之后的解释中称没有CO2参与,而CF3COHO充当羧酸盐源是由于CH4和CF3COHO之间更有利于热力学反应。非均相催化法大多采用两步、分步、周期或循环反应模式,以Co-Cu、V2O5- PdCl2/Al2O3、Pd amp; Rh/TiO2、Pd amp; Rh/SiO2、Pd/C和Pt/Al2O3 为催化剂,催化活性小于45 mu;mol/(g·cat ·h)的生成速率和较差的选择性。Huang等人提出了在双金属Co-Cu催化剂上合成乙酸的两步法,即伴随氢气吹扫,在循环之间交替投加二氧化碳和甲烷以得到各种含氧化合物,包括选择性较差的乙酸。Wang等人的研究表明,CO2比CO更适合通过介质阻挡放电形成。由二氧化碳直接合成乙酸是一个极具吸引力的反应。一些作者之前已经写过关于从二氧化碳和甲烷合成乙酸的可能性,特别是在金属沸石上,而对基本上从理论研究的可能性不予考虑。例如,Panjan等人从理论方法上探究了在Au-ZSM-5沸石上的反应。在Au-ZSM-5沸石上的碳氢键活化伴随着迅速发生的10.5 kcal/mol能阈的sigma;键活化均裂,以及由此产生的从金阳离子到沸石氧的质子交换,产生吸附在ZSM-5沸石的Broslash;nsted酸位点上的稳定的甲基-金络合物。进一步表明,在双功能催化剂上,CO2的转化包括在CO2质子化中起作用的Broslash;nsted酸位点和作为甲基化试剂的甲基-金络合物。Wu等人更是检验了由CH4/CO2在锌交换的H-ZSM-5上形成的酸性酸。他们证实锌位点能有效地激活甲烷,形成锌- 甲基基团(-Zn-CH3),并进一步受到二氧化碳的嵌入,产生表面乙酸衍生物(乙酸盐)。此外,Broslash;nsted酸位点被认为在质子转移到表面乙酸物种最终形成酸性酸中发挥了关键作用。在这两种情况下,都有一个甲基自由基中间体的发展形成(可能通过与金属和沸石笼的结合而稳定),然后与CO2反应,很可能是由与Broslash;nsted酸位点的相互作用引发。随后,用于二氧化碳甲烷化的催化剂是改变加入反应器的反应物化学结构的主要因素。
Zhang等人通过DFT-GGA计算铜(1 1 1)表面的形成研究甲烷和二氧化碳直接转化成乙酸,提出了bi-CH3COO的形成在动力学和热力学上比其他预测的途径更有利,bi-CH3COO的加氢可以通过Cu (1 1 1)的H 借助CO2和CH3分子的高放热反应来实现。Sangthong等人利用密度泛函理论(M06-L)研究了乙酸在Au-ZSM-5催化剂上的直接形成,提出了CH4在金阳离子位点的同分解解离,形成稳定的CH3-Au配合物和H-ZSM-5载体质子化CO2分子。Zhu等人通过傅里叶变换红外光谱证实了CHx和CHxO在铜/钴负载氧化物催化剂上的形成,Wu等人通过13C核磁共振证实了M-CH3的形成机理。最近,Narsimhan等人证明了使用铜交换沸石(ZSM-5和MOR)将CH4和CO2直接转化为乙酸是通过CH3O-MOR复合物的形成。然而,据我们所知,还没有关于在连续固定床反应器中同时进料由CH4和CO2直接合成乙酸的实验研究报告。在此,我们进行了下一步,首次在连续固定床反应器中使用铜交换的M-ZSM-5 (M = Li , Na , K 和Ca2 )将CO2和CH4一步催化转化为乙酸。金属铜物种和碱性阳离子作为双功能催化剂同时活化CH4和CO2以使乙酸能够连续形成的有益聚集效应得到了充分的讨论。
-
实验
- M-ZSM-5的制备
首先,在550 ℃条件下,将商品铵ZSM-5空气煅烧6 h以形成H-ZSM-5。然后,将H-ZSM-5 (1.0 g)在新鲜的50 mL (0.1 M) NaNO3溶液中悬浮3次,悬浮12 h。用热水/甲醇混合物彻底洗涤样品以除去吸附的盐。然后在110 ℃下干燥,在500 ℃对Na-ZSM-5进行5 h的煅烧。按照相同的方法制备其他样品以获得Li-ZSM-5、K-ZSM-5和Ca-ZSM-5。
-
- Cu-M-ZSM-5的制备
铜取代M-ZSM-5是在1.0 g M-ZSM-5 ,50 mL 0.25金属M离子的Cu(NO3)2·3H2O溶液中回流六小时进行的。滤出沉淀物,用去离子水彻底洗涤,真空干燥,并在550 ℃下煅烧5 h。在ZSM-5中用电感耦合等离子体显示的铜取代的M分别为22.1、15.6、20.2和16.1%,而在Cu-Li-ZSM-5, Cu-Na-ZSM-5, Cu-K-ZSM-5,和Cu-CaZSM-5中的扩孔阳离子分别为0.06、0.14、0.16和0.25%。因此,Cu-Li-ZSM-5, Cu-Na-ZSM-5, Cu-K-ZSM5, 和 Cu-Ca-ZSM-5中的Cu/M摩尔比分别为40.57、40.68、40.35和20.88。
-
- 催化剂的表征
粉末X射线衍射图(XRD)是通过用30 kV和15 mA,从5 °到90 °的CuKalpha;射线(lambda;=0.154 nm)的Rigaku Miniflex X射线衍射仪获得的。还原后的样品保存在惰性气体气氛和室温条件下,以避免CuOx的形成。 UV-vis-NIR漫反射光谱(DRS)是用岛津UV-2501 PC分光光度计执行的,该分光光度计配有反射附件,BaSO4用作参考材料。在室温下以反射模式记录近红外光谱。傅里叶变换红外光谱是用尼科莱冲击410光谱仪在400-4000 cm-1的范围内记录的。Brunauer, Emmett, and Teller (BET)催化剂的表面积是用广达铬AS1 Win、广达铬仪器v 2.01测量的。在进行这种测量之前,所有样品在实验前都在200 ℃下完全脱气6 h。X射线光电子能谱是用配备半球电子分析仪和铝阳极X射线激发源(AlKalpha;=1487.6eV)。样品的透射电子显微镜图像被记录在一台200 kV运行的JEOL JEM-2100(日本)上。在装有用于监测H2消耗的TCD检测器的常规流动系统中,用氢气(5 %体积分数的 H2混He)在50到600 ℃进行催化剂的程序升温还原(TPR),加热速率为10 ℃/min。
-
- 催化活性
甲烷和二氧化碳在装有适量催化剂(250 mg)的不锈钢固定床反应器中进行直接反应。用氦气(30 mL/min)在120 ℃下闪蒸催化剂30 min,以除去空气和湿气。随后,将氦气流切换到氢气(5 mL/min),并且使用温度程序在30分钟内将催化剂从30 ℃降低到400 ℃,并且在30 min内将温度进一步升高到450 ℃,恒定2 h。然后,在氢气流量为2 mL/min的条件下调节反应所需的温度。还原后,将摩尔比为2、1和0.5的甲烷和二氧化碳(1.5 mL/min)同时加入反应器,反应在425 ℃到525 ℃之间的不同温度下进行。测试参考煅烧样品以鉴定ZSM-5载体上的主要活性物种,然而,煅烧的样品对乙酸的形成没有显示出催化活性,表明主要的活性物质是Cu0。产品通过在线气相色谱(永林仪器,Acme 6000系列,韩国)进行分析,配有FID和TCD。
-
结果和讨论
- 筛选不同温度和不同甲烷与二氧化碳摩尔比下的催化性能
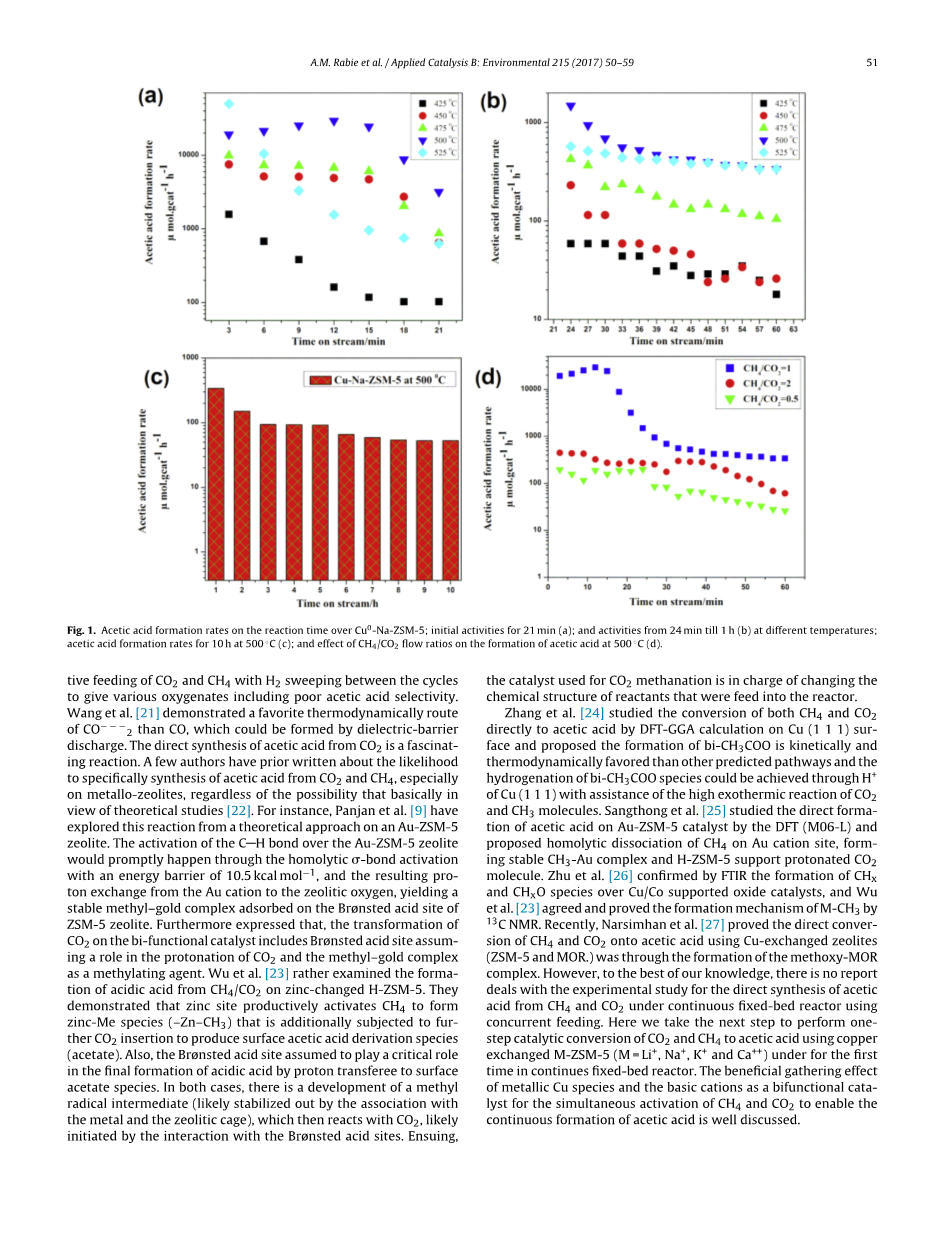
图1描述了随温度变化的乙酸生成速率;(a)起始到21 min的活性, (b)21 min后直1 h的活性;(C)500 ℃时的每小时活性和(d) Cu0-Na-ZSM-5催化剂上CH4与CO2流量比对的关系。在425-525 ℃之间对催化活性测试,乙酸形成的活性随温度升高而增加。令人关注的是,观察到乙酸稳定形成的最高温度为500 ℃,运行时间10 h。由于乙酸的形成直接取决于甲烷和二氧化碳的流量比,因此如图1d所示进行流量优化,在500 ℃,甲烷和二氧化碳的等摩尔流量比1:1时显示乙酸的形成速率最高。
图1 在Cu0-Na-ZSM-5上乙酸的生成速率与反应时间的关系;不同温度下起始到 21 min的活性(a);不同温度下24 min到1 h的活性 (b);在500 ℃下10 h的乙酸生成速率(c);500 ℃时CH4/CO2流量比对乙酸形成的影响(d)。
-
- 碱性阳离子的影响
为了了解碱性阳离子(M = Li , Na , K 和Ca2 )在Cuo-M-ZSM-5催化剂中的作用,在开始的第9分钟(图2a)、1 h(图2c)和10 h(图2d)时,将它们的活性与Cuo-H-ZSM-5催化剂活性图(图2)进行了比较。(图2b)显示了在第9分钟的初始阶段产生甲酸、甲醇和乙酸的产物分布,而在1 h后,乙酸的选择性约为100%。在整个反应温度范围内,Cu0-H-ZSM-5催化剂的转化率比其他碱性阳离子交换的Cult;
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[260869],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 播撒生物炭促进鸟粪石形成,但加速重金属积累外文翻译资料
- 钢铁工业余热有机朗肯发电的能量及炯分析外文翻译资料
- 深度共晶溶剂微波辅助处理木质素-碳水化合物复合 物的高效裂解及超快提取木质素低聚物外文翻译资料
- 功能化杯状芳烃离子团族[4]的合成、晶体结构及竞争结合性能外文翻译资料
- 面向高能量密度柔性超级电容器的无纺布用黑磷杂化微纤维的微流控纺丝结构外文翻译资料
- 活性炭对水溶液中氨的吸附外文翻译资料
- 制备可控海胆状NiCo2S4微球协同硫掺杂石墨烯作为高性能 二次锌空气电池的双功能催化剂外文翻译资料
- 钛酸盐材料对重金属离子的吸附外文翻译资料
- CO2敏感催化剂的合成与表征温度响应催化聚离子液体微凝胶外文翻译资料
- 温度响应微凝胶薄膜在湿环境中作为可逆二氧化碳吸收剂外文翻译资料


