
英语原文共 10 页,剩余内容已隐藏,支付完成后下载完整资料
基于多尺度斑点检测算法的自动乳腺超声图像计算机辅助肿瘤检测
Woo Kyung Moon,Yi-Wei Shen,孙敏裴,黄-生,陈全和,Ruey-Feng Chang *,IEEE高级会员
摘要
全自动全乳超声(ABUS)是检测乳房异常的新兴筛查工具。 在这项研究中,基于多尺度斑点检测的计算机辅助检测(CADe)系统被开发用于分析ABUS图像。 使用由136个乳房病变(58个良性病变和78个恶性病变)和37个正常病例组成的数据库测试所提出的CADe系统的性能。 斑点噪声降低后,采用多尺度斑点检测的Hessian分析应用于肿瘤的检测。 该方法检测到每个肿瘤,但也检测到一些非肿瘤。 使用基于blobness,内部回声和形态学特征的逻辑回归模型估计剩余候选者的肿瘤可能性。 肿瘤可能性高于特定阈值(0.4)的肿瘤候选者被认为是肿瘤。 通过将斑点,内部回波和形态学特征与10倍交叉验证相结合,所提出的CAD系统显示100%,90%和70%的灵敏度,每次通过的误报为17.4,8.8和2.7,分别。 我们的研究结果表明基于多尺度斑点检测的CADe系统可用于检测ABUS图像中的乳腺肿瘤。
关键词 - 自动乳房超声,斑点检测,计算机辅助检测,Hessian分析
一. 介绍
REAST超声(美国)可以用来补充乳房X线照相术,以提高密集乳房组织中乳腺癌检测的准确性[1],[2]。 但是,美国的手持式计算器非常耗时,结果强烈依赖于操作员。 美国筛查的使用也增加了活检的次数和良性病变的短期随访。 为了克服这些问题,已经提出了自动化整个乳房超声(ABUS)[3] - [9]。 凯利等人。 表明,使用ABUS和乳房X线照相术的乳腺癌检出率明显高于单独使用乳房X光检查在致密乳房组织[3],[4]。 与手持式美国[10]相比,ABUS不依赖于操作者,更省时,并且表现出更高的重现性[10]。 ABUS还提供三维图像,可用于多平面重建,以在工作站进行详细审查。 然而,这次审查需要医生投入大量时间,因为ABUS每乳房产生超过200张图像。 此外,内部回声较高的小病灶或与周围正常组织等回声的病变可能会被忽略 ABUS [5]。
为了帮助检查图像并形成ABUS数据的准确诊断,已经提出了计算机辅助检测(CADe)系统[7] - [11]。 池田等人。 [4]提出了一个利用边缘信息的CADe系统。 通过使用边缘和密度信息的分水岭算法对可疑病变进行分割。 分割后,使用二次判别分析来减少假阳性(FP)的数量。 该CADe系统的灵敏度为80.6%(29/36)
每个案例3.8个FP。 在Chang等人提出的CADe系统中。 [6],使用灰度切片方法对可疑病变进行分割。 为了区分肿瘤和FPs与可疑病变,基于规则的方法应用了七个特征。 CADe系统的灵敏度为92.3%(24/26)每箱1.76个FPs。 以前CADe系统在美国图像中检测乳腺肿瘤的大多数研究[4],[6],[11] [12]使用强度信息来分割可疑肿瘤。 然而,基于强度阈值方法的CADe系统的肿瘤检测并不总是成功的,特别是对于具有高内部回波损伤的美国图像。 具有较高内部回波的病变可能会通过强度阈值方法分割成几个分散的区域。 另外,美国图像中一些具有相邻阴影的病变可能会通过强度阈值方法过度分割。 对于3D ABUS图像尤其如此。
以上,病变可能由强度阈值方法分割不良,导致CADe系统的性能下降。
Hessian分析已被用于检测几种常见的几何结构,如血管,斑点和板[13] - [16]。 Frangi [14]提出了一种基于Hessian分析的血管增强滤波器,该滤波器计算图像的二阶局部导数,并根据这些局部导数的所有特征值的基础测量血管。 基于Hessian的斑点检测也被用于检测MRI图像中的前列腺病灶,并显示出高灵敏度和合理数量的FP [16,17]。 然而,据我们所知,斑点检测算法尚未应用于乳腺病变。 在ABUS图像中存在的乳房病变在几何模型中可以被认为是暗斑状结构。 我们的假设是基于Hessian分析的斑点检测可以改善低对比度边界或附近阴影的乳腺病灶的分割。
在本文中,基于多尺度斑点检测算法的CADe系统被提出用于检测ABUS图像中的乳房病变。 该算法的性能是针对包含各种乳房病变的数据库以及正常病例进行测试的。
二. 材料
在2007年6月至2008年6月在首尔国立大学医院使用SomoVu ScanStation(U-system,San Jose,CA)获取ABUS图像。 SomoVu ScanStation由一个View Station和一个扫描站组成。 扫描站以10-MHz线性换能器扫描仰卧位患者,宽度为15.4厘米。 获取的数据然后被传送到View Station。 所获得的三维图像的像素分辨率在横向上为0.285mm,
矢状方向0.086毫米,冠方向0.6毫米。 尽管这种换能器比传统换能器更宽,但仍然无法一次覆盖患者的整个乳房。 每位患者的一根乳房分两次或三次扫描以覆盖整个乳房。 病变患者仅使用一次。 活检证实136个病灶(大小范围:0.5-6.5cm,平均标准偏差: 厘米)从122例患者。 在136个病灶中,58个是良性的(27个纤维腺瘤和31个纤维囊性病变),78个是恶性的(71个浸润性癌和7个原位导管癌)。 作为对照,包括37个ABUS通过,没有异常发现。 因此,总共有159个病例(122个异常病例和37个正常病例)用于评估所提出的CADe系统的性能。 本研究得到了我们的机构审查委员会的批准。 知情同意书被免除。
三. 方法
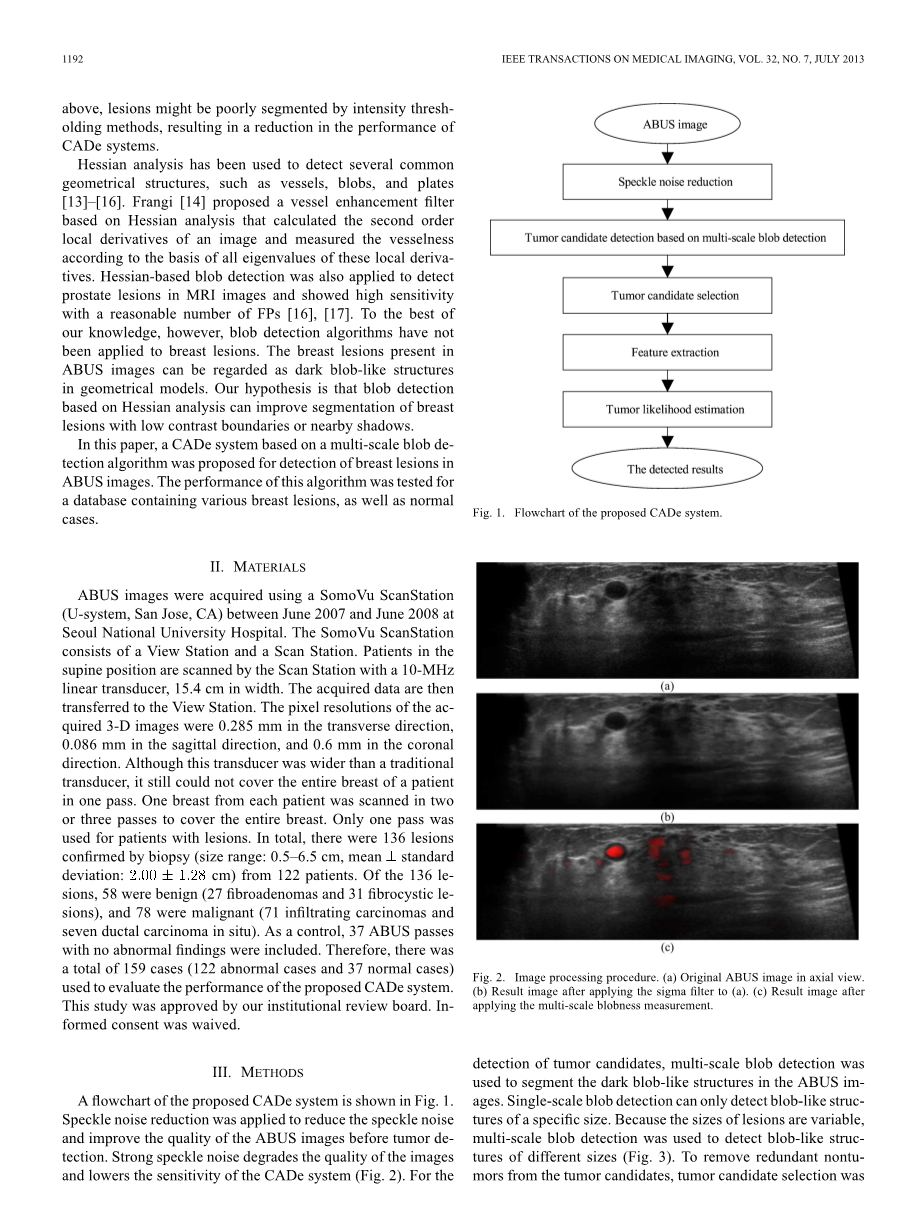
提出的CADe系统的流程图如图1所示。斑点噪声降低被应用于减少散斑噪声并提高肿瘤检测前ABUS图像的质量。 强烈的散斑噪声会降低图像质量并降低CADe系统的灵敏度(图2)。
图2.图像处理程序。 (a)轴向视图中的原始ABUS图像。
(b)将sigma;滤波器应用于(a)后的结果图像。 (c)应用多尺度污点测量后的结果图像。
为了检测肿瘤候选者,使用多尺度斑点检测来分割ABUS图像中的黑斑样结构。 单尺度斑点检测只能检测特定尺寸的斑点状结构。 因为病变的大小是可变的,所以使用多尺度斑点检测来检测不同大小的斑点状结构(图3)。 为了从肿瘤候选中去除多余的非肿瘤,选择肿瘤候选者应用。
图3.单一和多尺度斑点检测的检测结果。 (a)两个箭头指示内部回声高的病灶。 (b) - (f)使用单尺度斑点检测/的检测结果,以及3.2 mm。 (g)具有多尺度斑点检测的检测结果。 (h)使用多尺度斑点检测的检测边界。
使用具有斑点,内部回声和形态学特征的逻辑回归模型估计剩余肿瘤候选者的肿瘤可能性。 最后,通过对肿瘤可能性应用不同的阈值来评估所提出的CADe系统的性能。
A. 散斑降噪
为了消除斑点噪声并保留边缘信息,使用了边缘预防平滑滤波器[13],[18]。 应用西格玛滤波器[18]去除斑点噪声,同时保留边界信息。 西格玛滤波器采用均值和标准差的高斯分布。 通过对一个范围内中心的相邻像素进行平均,可以计算出二西格玛平均值
然后可以计算该范围内中心的相邻像素的位置。 当数字时,中心像素的强度值被计算的二西格玛平均值代替 在两个西格玛范围内的中心的相邻像素的像素大于特定阈值或当不满足上述条件时的相邻像素的平均值。 应用西格玛过滤器后的结果可能与平均过滤器相似。 某些边缘信息可能会在高时被删除 值被使用。 在我们的实验中值用3x3x3内核设置为3以消除斑点噪声。 图2(a)和(b)分别显示了应用斑点噪声降低之前和之后的二维图像切片。
1) 基于多尺度斑点检测的肿瘤候选检测:采用Hessian分析来增强几种几何结构,包括管状,斑点状和板状结构[14-16]。 该分析的原理是通过用高斯内核的导数将ABUS图像卷积来计算沿三维方向的二阶导数。 Hessian矩阵由以下公式定义:
(1)标度表示高斯分布的标准偏差并且表示沿方向th和th的第二偏差。 比例尺可以用来控制增强斑点状结构的半径。 当使用高规模价值时,大型斑点状结构得到增强。 特征向量和特征值
可以通过在每个像素处求解Hessian矩阵来计算。 计算出的特征向量表示检测到的物体的三个正交方向,特征值表示沿着相应方向的曲率程度。 为了增强ABUS图像中的暗斑状结构,可以将像素结构的可能性和像素的特征值的大小表述如下:
其中代表类似斑点结构的可能性并表示像素的特征值的大小。 在斑点状结构中,沿着三个正交方向的曲率应该高且相似。 因此,当物体类似于斑点状结构时,可以达到最大值。 一般来说,物体特征值的大小通常大于背景的大小。 因此,可以用来区分对象和背景。 使用以下公式可以增强斑点状结构:
其中表示位置/处的特征值和分别表示项和的灵敏度参数。 灵敏度参数可以控制相应术语的权重。 在我们的研究中,灵敏度参数设置为0.5。 这种情况只能增强黑暗的物体。 因为病灶通常有不同的大小,一个单一的尺度无法检测到所有病变。 为了检测不同尺寸的病变,可以使用多尺度血块测量。 公式如下:
比较单一和多尺度斑点检测的结果(图3)。 在ABUS图像中,与大规模检测相比,小尺寸斑点检测更好地分割更精细的病灶边界,其中病变被分割成多个分割区域。 大规模的斑点检测可以将病变的主要部分分割为高内部回波,但分割结果比小尺寸斑点检测粗糙。 在我们的实验中,多尺度斑点检测的范围从1.2到3.2毫米。 图2(c)显示了应用多尺度污点测量后的结果。 最后,采用连通分量标记[19]将增强像素分组到肿瘤候选区域。
2) 肿瘤候选物选择:在肿瘤候选物检测之后,由于肿块测量的高灵敏度,肿瘤候选物包括许多冗余的非肿瘤。 如果使用所有候选肿瘤来提取特征并估计肿瘤可能性,则处理可能需要很长时间,并且由于FP的高频率,CADe系统的性能可能较差。 因此,采用肿瘤候选者选择来消除来自候选肿瘤的FP。
高blobness值表明该候选人类似于一个黑斑般的结构[16]。 非肿瘤可能具有比可疑病变更低的斑点值。 因此,使用以下公式来使用肿瘤候选者的平均值和最大斑点值来消除FP:
哪里 代表具有总体/体素的肿瘤候选者并且指示体素属于该体素 肿瘤候选人。 用于肿瘤选择的另一个特征是肿瘤候选者的大小(大小)。 因为基于Hessian分析的肿瘤检测对强度变化敏感,所以许多小区域也被检测为肿瘤候选者。 这些区域通常比真实病变小,它们的大小可以用来消除病变,
从肿瘤候选人中筛选出许多FP。
对于肿瘤候选者选择,应用线性回归模型[20]从肿瘤候选者中消除FP。 肿瘤选择功能/如下:
最后,肿瘤选择标准可以表示如下:
其中TH是确定来自FP的剩余肿瘤候选者的阈值。 当通过肿瘤选择模型估计的值等于或大于TH时,检测到的区域保持为肿瘤候选者。 当通过肿瘤选择模型估计的值小于TH时,将检测到的区域从肿瘤候选中去除。 在我们的实验中,肿瘤标准阈值设定为0.5。
3) 特征提取:在选择肿瘤候选者之后,大多数FP从肿瘤候选者中消除。 但是,剩下的肿瘤候选人仍然存在一些非肿瘤。 为了进一步提高CADe系统的性能,提取了三个特征组(blobness,内部回声和形态学)以估计剩余肿瘤候选者的肿瘤可能性。
a) Blobness特征:由于肿瘤通常比ABUS周围的组织更暗,所以肿瘤比其他组织更类似于黑斑样结构。 因此,斑点值可用于区分剩余肿瘤候选者中的非肿瘤和肿瘤。 在我们的研究中,斑点值的最大值,平均值和标准偏差被用作斑点特征。 另外,当体素位置更接近肿瘤候选者的中心时,真实肿瘤的体素的斑点值可能更高。 因此,真正的肿瘤可能在肿瘤候选者的中心和相对于其他组织的斑点质心之间具有较小的距离。 在这项研究中,肿瘤候选者的中心与斑点质心之间的距离被用作特征。 肿瘤候选者/的中心可以表示如下:
其中/表示体素在肿瘤候选者中的位置。 Blobness质心/可以表述如下:
其中I表示肿瘤候选者中斑点值的总和,并且/表示体素的特征值。 最后,如图4所示,肿瘤候选者的中心与斑点质心之间的距离可以定义如下:
图4.肿瘤候选者的中心和斑点质心之间的距离被定义为斑点特征。 在此示例中,高Blobness值汇总在椭圆的右下角。
b) 内部回声特征:在美国的乳腺肿瘤诊断中,内部回声模式是区分良性肿瘤和恶性肿瘤的有用特征[21]。 在我们的研究中,应用内部回声特征来区分肿瘤和其余肿瘤候选者中的非肿瘤。 在内部回声特征中,肿瘤候选者的强度分布的均值,标准偏差,偏度和峰度[22]可以定义如下:
其中/是属于具有总体/体素的肿瘤候选者的位置中的体素的强度。 此外,内部回声特征也使用均值,强度梯度的标准偏差和病灶边界强度梯度的平均值。
c) 形态学特征:形态学和形态学特征可以为肿瘤诊断提供有用的信息,并且已被证明对计算机辅助诊断(CADx)系统的应用有效[7]。 在我们的研究中,这些特征被用来区分肿瘤和其余肿瘤候选者中的非肿瘤。
我们研究的形态特征包括两类:形状和椭圆拟合[7]。 对于形状特征,包括体积,半径,针尖[23]和两个三维紧致特征[24]。 用半径和针尖来描述病变的边缘特征,并用两个三维致密特征来表征病变表面和病变体积之间的关系。 传统的和新的紧凑性特征可以描述如下:
其中Surface表示肿瘤候选者的表面,Volume表示肿瘤候选者的体积。 椭圆拟合特征用于描述肿瘤候选者的规则程度。 本研究中使用的特征已在别处进行了描述[7]。
4) 肿瘤似然估计:为了区分肿瘤和非肿瘤,使用逻辑回归模型[20]来使用上述特征对肿瘤和非肿瘤进行分类,并估计剩余肿瘤候选者的肿瘤可能性。 为
全文共10694字,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[15309],资料为PDF文档或Word文档,PDF文档可免费转换为Word


