
英语原文共 8 页,剩余内容已隐藏,支付完成后下载完整资料
使用红毛丹果皮中的提取物生物合成纳米氧化锌粒子及氧化锌粒子的对甲基橙染料光催化活性
Thenmozhi Karnan, Stanly Arul Samuel Selvakumar
Department of Chemistry, University College of Engineering Kanchipuram, Tamil Nadu 631 552, India Department of Applied Chemistry, Sri Venkateshwara College of Engineering, Sriperumpudur, Tamil Nadu 602 117, India
摘要:在本文中,具体描述了通过生物合成方法使用红毛丹果皮提取物合成氧化锌纳米颗粒,并且开发了一种新的低成本技术制备氧化锌纳米颗粒。在合成过程中,果皮提取物作为一种天然的绑定剂。将使用这种方法成功制备的产品进行了分析与一些标准的表征研究,如X射线衍射(XRD)、紫外-可见漫反射率光谱(UV-Vis DRS),场发射扫描电子显微镜(SEM),高分辨透射电镜(HR-TEM)、N2吸附-脱附等温线和UV-Vis吸收光谱等。以甲基橙降解实验研究了ZnO纳米粒子的光催化活性染料(MO)在紫外光下的脱色效率,结果表明有83.99 %左右的粒子在120分钟光照下脱色。除了脱色,矿化也发生了。矿化现象已经通过测定化学需氧量(COD)值被确认了。
关键词:纳米氧化锌,生物合成法,光催化活性,甲基橙,紫外光线
1. 引言
有毒的提取物染料会通过纺织厂严重影响水生生态系统,造成环境污染。近年来,半导体基光催化剂引起了广泛的关注,因为它提供了一个潜在的解决环境问题的方法。迄今为止,许多半导体材料已被评估为光催化剂。氧化锌是一种重要的宽禁带半导体(3.37 eV),由于其独特的电学和光学特性而备受关注.。氧化锌具有广泛的应用,如如光催化、太阳能电池、化学传感器、压电传感器、透明电极、电致发光器件的广泛,紫外激光二极管、光电器件、激光技术、抗菌活性等。制备氧化锌有多种方法,主要包括沉淀法,水热法,微乳法,微波法,溶剂热法,非水溶液合成法,草酸盐前驱体乳液沉淀热分解法等。虽然这些技术已可以成功制备纳米氧化锌粒子,但还需要的有毒化学物质作为盖髓剂,精良的设备、繁琐的程序和严格的实验条件等要求。因此,现在有很大的必要去探索新的合成方法,从而克服现存的困难。使用植物提取物通过生物合成的方法制备纳米氧化锌粒子的方法是个鼓舞人心的发现。因为这种方法是容易,干净,无毒,环保,节省成本,无副产品并且提供了天然的覆盖剂的方法。通过查阅文献,用绿茶,扶桑,印楝,芦荟,大蒜叶,龙葵叶,香草叶等的植物提取物生物制备氧化锌的方法已被发现。
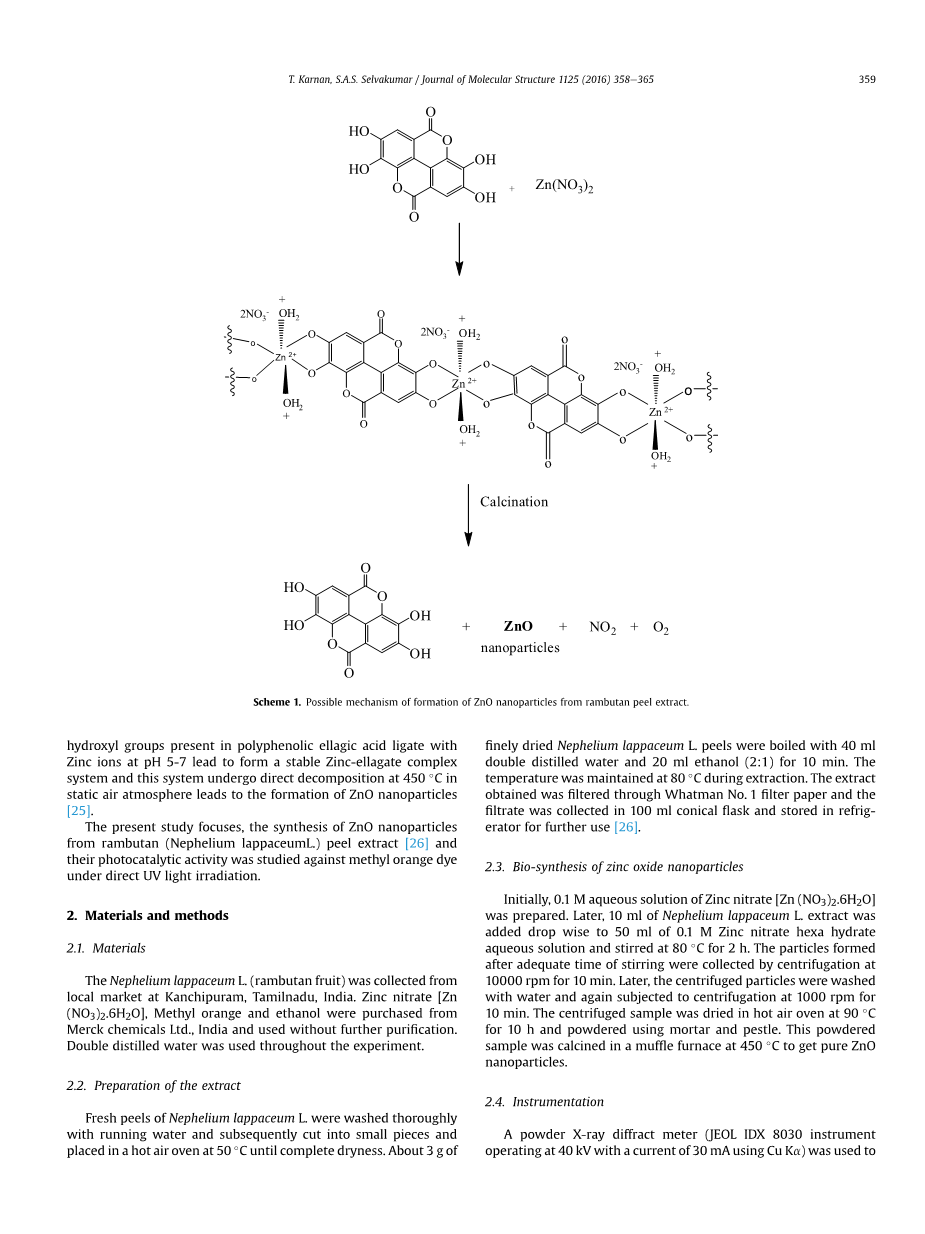
方案1.从红毛丹果皮提取物形成的ZnO纳米粒子的可能机制。
在目前的工作中,我们描述了用红毛丹表皮的提取物生物合成纳米氧化锌粒子的方法。红毛丹是一种与荔枝和龙眼相似的热带无患子科的水果。鞣花酸,柯里拉京,格拉宁和鞣花单宁是存在于红毛丹内的原发性较高的酚类物质。使用红毛丹果皮提取物制备纳米氧化锌的实施方案.1。在这里,植物提取物作为绑定剂使用。芳香族羟基与多酚鞣花酸与锌离子在pH为5-
7形成一个稳定并且复杂的锌-鞣花体系,并且这个体系在450 ℃静态空气气氛下分解形成纳米氧化锌粒子。
本研究的重点在于,用红毛丹表皮的提取物生物合成纳米氧化锌粒子的方法和合成出的产品使用对甲基橙染料在紫外光照射下对其光催化性的研究。
2. 材料与方法
2.1. 材料
红毛丹是在印度泰米尔纳德邦的坎奇普兰的当地市场收集的。硝酸锌,甲基橙和乙醇从印度默克化工有限公司购买的,并且没有使用进一步净化的阳离子水。整个实验采用双蒸馏水。
2.2. 提取液的制备
用自来水清洗新鲜的红毛丹表皮,随后切成小块,并且放在50 ℃的热烘箱中直至完全干燥。取约3 g完全干燥的红毛丹果皮放入40 ml蒸馏水和20 ml乙醇(2:1)的混合液中煮10 min。在提取过程中的温度保持在80 ℃。得到的提取液使用Whatman一号滤纸过滤,并且用100 ml锥形瓶收集滤液,将滤液放在冰箱中以备后用。
2.3. 氧化锌纳米粒子的生物合成
一开始,制备0.1 M硝酸锌溶液。接着将10毫升红毛丹果皮提取液加入50毫升0.1 M硝酸锌溶液中,在80 ℃下搅拌反应2 h。经过充分的搅拌形成颗粒,混合液使用离心机在10000转下离心10 min。接着,离心出的产物用清水洗净,再重复上述步骤。离心出的样品在90 ℃烘箱中干燥10 h,随后用研钵和杵将样品磨成粉。将所得粉末放入马沸炉中煅烧得到纯氧化锌纳米颗粒。
2.4. 仪器仪表
粉末X射线衍射仪用了测定样品中是否存在结晶相。UV-VISe 岛津漫反射分光光度计用于光催化性能的研究,在200至800 nm波长范围内使用硫酸钡作为标准。德国,卡尔蔡司的热场发射扫描电子显微镜和高分辨透射电镜用于观察粉末的表面形貌。麦克ASAP 2400比表面积分析仪用于测定表面积。SHIMADZUUV-1650PC紫外可见分光光度计用于记录对甲基橙溶液的降解。
2.5. 光催化活性
光催化实验是在三个不同的条件下对比进行的:一,在光照条件下无催化剂;二,再无光照条件下有催化剂;三,在光照条件下有催化剂。选用10 mg/L 的水溶性偶氮染料甲基罗伦吉作为模型污染物。其pH值为7.01。光催化活性通过甲基罗伦吉染料在紫外光下的降解情况来测定。使用一个8 W的高压汞蒸气灯作为辐射源。将100 mg生物合成的氧化锌纳米粒子加入100 ml甲基橙水溶液中,并且磁力搅拌至混合均匀无气泡。在光照前,反应液在黑暗条件下磁力搅拌超1 h,以确保催化剂和染料之间的吸附/解吸平衡的建立。在等待过程中,取3 ml的悬浮液,将其过滤,并用微冷却离心机在6000转速下转20 min,去除光催化剂。离心后的甲基橙使用UV-Visible分光光度计在464 nm下进行吸光度分析。在脱色的结束,其脱色效率通过下列公式计算,
Ao是在照射前的吸光度,At是照射t时的吸光度。在确保染料脱色完全后,成矿作用采用化学需氧量(COD)还原法用COD值来测定。预估价和光催化后的染料的COD值用标准重铬酸钾标记,并用COD消化。
3. 结果与讨论
3.1. XRD图谱
用XRD图谱表示所制备的样品的结晶相,如图1所示。不同的衍射峰在2倍theta;角为31.71°、34.38°、36.21°、 47.52°、 56.54°、62.84°、 66.23°、67.95°、 69.05°、72.53°和77.14°分别对应 (100), (002), (101), (102), (110), (103), (200), (112), (201), (004) 和(202)平面。在图1中,所有的衍射峰很好的对应了氧化锌的六角相,这是非常接近标准值的。尖锐的和窄的峰,表明纳米粒子高度结晶。通过Debyee-Scherrer公式来计算纳米颗粒的晶粒尺寸,
这里K是谢勒常数(0.94),L是X射线波长(0.1541 nm),beta;是半峰宽度,theta;是布拉格衍射角。平均晶粒尺寸D的计算采用公式(1),其被认为是25.67 nm。
图1.合成的ZnO纳米粒子的XRD图
3.2. 扫描电镜分析
图2.物纳米ZnO 扫描电镜图像。
图2显示粒子的大小和生物纳米氧化锌的形貌。从SEM图像显示,这是由于纳米团簇聚集形成的纳米粒子聚集点。纳米颗粒是球形的,其粒径在25~40 nm,这和已发现的十分相似。颗粒的均匀、分散性很好。粒径均匀的光催化剂可以有效地提高光催化反应的效率。
3.3. 透射电子显微镜分析
图3.(a)ZnO纳米粒子的透射图像(b)纳米颗粒的粒径分布直方图。
通过不同大小的阳离子进行HR-TEM分析,为氧化锌纳米结构的形成提供了进一步的证据。图3是典型的纳米氧化锌HR-TEM图像,表明纳米颗粒具有球形形貌和自组装。范德华力和静电相互作用的集体作用将有利于我们从从电子显微镜研究观察自聚集/自组装的纳米氧化锌。
3.4. BET比表面积分析
一般来说,一个好的比表面积对对催化剂的活性有良好的影响。在本实验中,用表面积是69.01 m2/g的球形氧化锌纳米颗粒。好的比表面积的氧化锌通过提高甲基罗伦吉的吸附作用来促进光催化活性,这是决定性的一步催化反应。
3.5. 紫外线-可见漫反射光谱
图4.生物合成ZnO纳米粒子的紫外-可见光谱。
通过紫外可见漫反射光谱对纳米氧化锌粒子的光学性质进行了研究,其图谱如图4它清楚地表明,生物氧化锌纳米粒子的吸收边缘位于约373 nm,证明了纳米氧化锌粒子可以被紫外可见光激发。氧化锌从波长值对应于光谱的垂直和水平部分的交点的带隙能量,使用下列方程计算。
方程式中,Eg是带隙能量,h是普朗克的常数,C是光速,lambda;是波长。从图4看,用方程式计算吸收边缘被定位在约373 nm处的带隙值,为3.32 eV。宽带隙显然是由小的平均粒径决定的。
3.6. 红外光谱分析
为了确定生物合成氧化锌纳米粒子中的有机物种的存在,我们进行了红外光谱研究,光谱图如图5所示。强烈的吸收带在3439 cm-1,1629 cm-1, 1383 cm-1,446 cm-1,分别是因为O-H伸缩振动,因吸潮H-O-H弯曲振动,-C-O和C-O-C拉伸振动和Zn-O伸缩振动导致的。观察到的其余的频带约2404 cm-1,163 6cm-1,816 cm-1和637 cm-1,可能是由于存在一些生物分子作为连洗绑定剂的原因。
图5.生物合成ZnO纳米颗粒的红外光谱。
3.7. 光催化活性研究
3.7.1. 紫外光谱分析
以甲基橙为模型污染物,在紫外光直接照射下,进行生物合成氧化锌纳米颗粒的光催化活性的研究。MO是一种含磺酸盐和偶氮基团的偶氮染料。在实验中,偶氮基将作为发色基团,产生强烈的橙色。在氧化锌纳米颗粒被紫外光直接照射期间,强烈的橙色逐渐转变为无色,如图6(a)所示。这是由于发色基团与有机染料被光分解破坏。
通过使用紫外-可见光谱(200 nm至600 nm)进一步研究证明MO在不同时间间隔溶解,由图6(b)显示。为了研究光催化剂的稳定性,MO溶液第一个进行光解过程研究。结果表明,在光解过程中,只有6 %在光亮中降解,只有约7 %在黑暗中降解。降解使用结果表明在光亮中与在黑暗中降解相近。没有检测到的变化发生。这意味着光催化剂和光对于光催化反应的加速是必要的。图6(b)
图6.(a)染料颜色由橙色逐渐变为无色。(b)随反应时间光催化降解图谱。(c)钼溶液作为不同时间间隔函数的降解。
显示在464 nm处MO染料具有强吸收最大值,这是由于其有色集团和它的紫外曝光时间增加到120分钟,并且达到83.99 %时降解效率降低。这清楚地说明了发色基团裂解。图6(b)显示了由于MO去氨基,从464 nm到442 nm发生蓝移现象。
如图6(c)所示,为染料浓度随时间变化的曲线图。120 min后,由于光催化反应生成羟基自由基的氧化反应的发生,约83.99 %的MO在紫外光下被降解。详细机制见Scheme.2。甲基橙溶液对氧化锌纳米颗粒在不同的反应条件下的光降解效率如表1所示。我们将我们的研究结果与其他植物提取物制备的氧化锌和其他植物提取物制备的氧化锌进行比较,并给出了表2的结果。氧化锌纳米颗粒成功分解为甲基橙偶氮染料,并且形成毒性较低的终端产品如二氧化碳,二氧化氮和一氧化氮等。
方案2.生物合成ZnO纳米颗粒的光催化反应机理。
表1同反应条件下的纳米氧化锌钼溶液的光催化降解效率。
表2不同方法制备的ZnO纳米粒子的光催化活性比较。
3.7.2. 钼染料的矿化研究
为了确认矿化效率,降解部分采用COD值进行评价。测定光催化处理前和后的COD值。在紫外线照射120 min后,COD值从6162 mg / L 减少为 481 mg/L。COD值的减少用来确认生物合成氧化锌纳米粒子降解效率。
- 结论
目前,使用红毛丹表皮提取物为原料制备已成功制备纳米氧化锌微粒。使用X射线衍射仪确定了其结晶相,使用紫外漫反射光谱确定了其能量带隙,为3.32 eV 。制备的球形纳米氧化锌粒子的粒径由FESEM和HR-TEM确定,为25至40 nm。其表面积测定为69.01 m2/g,同时显示了良好的光催化活性。使用甲基橙测定其光催化降解效果,结果表明,在紫外光照射120
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[486592],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 基于环氧树脂的超疏水结构防腐涂层外文翻译资料
- 田口优化技术在确定薄壳类零件注塑成型工艺参数中的应用外文翻译资料
- 形状和尺寸控制的钼酸钙甜甜圈形微结构的合成外文翻译资料
- 纳米多孔钴基ZIF-67金属有机骨架(MOF)在构建具有优异防腐性能的环氧复合涂层中的应用外文翻译资料
- 田口方法在塑料注射模具设计中减少翘曲的应用外文翻译资料
- 浸渍和封装轻质骨料用于自修复混凝土的研究外文翻译资料
- 具有形状恢复和超吸收特性的化学交联纤维素纳米晶体气凝胶外文翻译资料
- 一锅法合成非贵金属WS2/g-C3N4增强型光催化剂制氢外文翻译资料
- 由MOF-74 (Zn)制备具有超快吸附污染物能力和超电 容特性的多功能多孔Zn0-C复合材料外文翻译资料
- 氢键控制的柔性共价有机骨架的结晶度和吸附 性能的机理研究外文翻译资料


