
英语原文共 7 页,剩余内容已隐藏,支付完成后下载完整资料
基于三线态敏化上转换的体内纳米温度比率探针
摘 要
温度是生命系统的重要因素,复杂的生命活动通常与温度有关。基于非接触光学原理的体内温度测试将有利于揭示其背后的生理现象,同时将对生物体的影响最小化。在此,一种基于三线态-三线态湮灭(TTA)机制的高热敏感上转换机理被开创性地应用于在生理温度范围内敏感地指示体温变化。将具有近红外(NIR)发射且对温度不敏感的NaYF4:Nd纳米荧光粉掺入到温度响应性TTA上转换系统中以用作内部校准单元。因此,开发一种能够精确监测体内温度变化的温度比率探针,具有高热灵敏度(约7.1% K-1)和分辨率(约0.1 K)。
近年来,发光纳米热学受到了广泛的关注,因为它具有广泛的应用领域,涉及纳米医学、微流体、纳米电子学和集成光子器件。这种高灵敏度纳米温度探针在相关领域的发展非常重要,特别是在诊断和治疗方面具有巨大的革命潜力。近年来,体内温度监测被认为是生理学、医学诊断和可控热疗研究的一个有用工具。基于发光成像的非接触式温度测量为体温的绘制提供了一种无创、可观察的方法。值得注意的是,基于反斯托克斯过程的上转换可以避免生物系统的自体荧光,是体内温度探针发展的一种有前景的技术。在此背景下,基于镧系元素的上转换纳米荧光粉(UCNPs)的温度探针被开发出来。然而,基于UCNPs的温度探针通常表现出中等的热灵敏度(lt;1.6% K-1)和分辨率(gt;0.5 K),以及较差的发光效率。因此,迫切需要一种能够监测体内微小温度变化的高灵敏度温度探针。
作为最有效的反斯托克斯过程,基于三线态-三线态湮灭(TTA)的上转换过程具有潜在的热敏性。TTA上转换涉及到发光剂和光敏剂双组份中的多重能量转移。直观地说,TTA上转化需要分子发色团的扩散,这对细微的温度变化是很敏感的。然而,基于TTA上转换技术的体温计在体内的应用尚未报道,这主要是由于生理环境中温度响应不规则或热灵敏度低、浓度依赖性严重等重大挑战的阻碍。
在此,我们优化设计了一个TTA体系来探索体内温度探针。在较高的温度下,发光剂的扩散速率和碰撞概率的提高使TTA的上转换率急剧提高。在我们的设计中,除了抑制非辐射失活外,上转换发光(TTA-UCL)在生理温度范围内与温度呈正相关(补充图1)。为了最大限度地减少生物环境的影响,并使指示信号的浓度独立输出,TTA发色团用热敏感内标封装(补充图2)。参考文献显示,第二个生物窗口的近红外辐射也适用于生物成像。因此,实现了TTA-Nd-NPs作为比例温度探针(图1)。通过准确测量组织中的温度分布以及检测炎症引起的小鼠温度变化,证明了TTA-Nd-NPs在体内比例测温中的潜在用途。这项工作对于上转换、温度测量、纳米医学和生命科学的广泛研究领域意义重大。
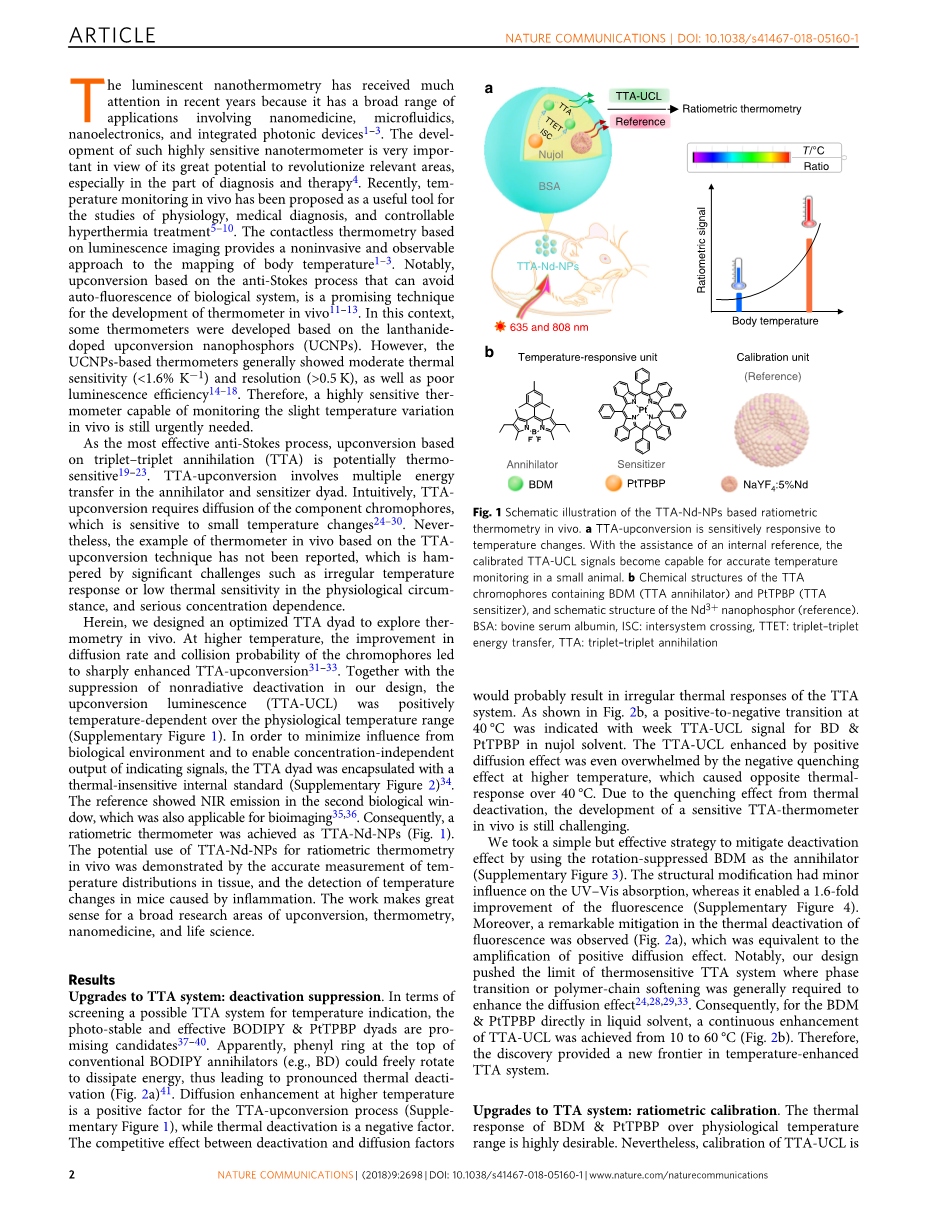
图1 基于TTA-Nd-NPs的体内比率测温法的示意图。 TTA上转换对温度变化敏感。 在内部参考的帮助下,校准的TTA-UCL信号能够在小动物中进行准确的温度监测。 b含有BDM(TTA激活剂)和PtTPBP(TTA敏化剂)的TTA发色团的化学结构,以及Nd3 纳米荧光粉(参考)的示意结构。 BSA:牛血清白蛋白,ISC:系统间杂交,TTET:三线态-三线态能量转移,TTA:三线态-三线态湮灭
实验结果
图2在TTA体系中实现高度正热响应的策略。 a结构修饰,从而抑制荧光的热失活。 b分别从BDM和PtTPBP以及BD和PtTPBP发射的TTA-UCL信号的温度响应。 当抑制负失活效应时,正扩散效应变得更强,以产生具有高灵敏度的正温度响应趋势。 使用635 nm激光(100 mWcm-2)作为激发源。 石蜡液中BDM,BD,PtTPBP和L-抗坏血酸6-棕榈酸酯的浓度分别为1times;10-3 M,1times;10-3 M,5times;10-5 M和1 mg mL-1。
TTA体系优化:失活抑制。在筛选可以作为温度指示的TTA体系方面,光稳定且有效的BODIPY和PtTPBP双组份是有希望的候选。显然,常规BODIPY湮灭剂(例如BD)顶部的苯环可以自由旋转以耗散能量,从而导致明显的热失活(图2a)。在较高温度下的扩散增强是TTA上转换过程的积极因素(补充图1),而热失活是一个消极因素。失活和扩散因子之间的竞争效应可能导致TTA体系的不规则热响应。如图2b所示,在40 ℃下的正-负转变表示在石蜡溶剂中BD和PtTPBP的周TTA-UCL信号。正扩散效应增强的TTA-UCL甚至被较高温度下的负猝灭效应所掩盖,在40℃以上产生相反的热响应。由于热失活的猝灭效应,在体内开发灵敏的TTA温度探针仍然具有挑战性。
我们采用了一种简单但有效的策略,通过使用旋转抑制BDM作为湮灭剂来减轻失活效应(补充图3)。结构修饰对紫外-可见吸收的影响很小,而荧光强度则提高了1.6倍(补充图4)。此外,观察到荧光热失活的显着缓解(图2a),这相当于正扩散效应的放大。值得注意的是,我们的设计突破了热敏TTA体系的极限,其中通常需要相变或聚合物链软化来增强扩散效应。因此,对于直接在液体溶剂中的BDM和PtTPBP,在10至60 ℃下实现TTA-UCL的连续增强(图2b)。因此,该发现为温度增强的TTA体系创造了新的领域。
图3 TTA-Nd-NPs的性质研究。 a TTA-Nd-NPs在不同激发功率下的双发射特性。 TTA-UCL信号在540 nm处达到峰值,并且在1060 nm处达到峰值的参考信号被绘制在发射谱中。 插图:用磷钨酸钠负染色后TTA-Nd-NPs的透射电子显微镜图像。比例尺为200 nm。b 精确控制温度下校准TTA-UCL测量设置的示意图。 c TTA-Nd-NPs在水溶液中的热敏感性。 用635 nm(100 mWcm-2)和808 nm(100 mWcm-2)耦合激光器的激发下测量光谱。 插图:TTA-UCL(Em I,绿线)和参考信号(Em II,红线)的综合发射强度作为温度函数。 d室温下浓度对比探测法(蓝线)和强度基的探法(绿线)的影响
TTA体系优化:比率校准。BDM和PtTPBP在生理温度范围内的热响应是非常理想的。然而在复杂的生物系统中,TTA-UCL的校准仍然是测温的必要条件。因此,在本研究中将校准单元引入TTA体系。通过在高压均化器中自组装BDM和PtTPBP和beta;-NaYF4:5%Nd(补充图5)来制备TTA-Nd-NPs材料。校准信号(Nd3 的4F3/2-4I11/2)与TTA-UCL的重叠最小,避免了串扰效应(补充图2)。在透射电子显微镜图像中显示了有机-无机TTA-Nd-NPs的纳米复合结构,直径约160 nm(补充图6)。TTA-Nd-NPs的流体力学半径为165 nm,并且尺寸在10-50 ℃内保持不变(补充图7)。此外,在生物相容性研究中未发现TTA-Nd-NPs材料的明显毒性(补充图8)。
TTA-Nd-NPs中的TTA双组份BDM和PtTPBP产生绿色上转换发射,寿命为170 mu;s(补充图9),室温下绝对量子效率为3.1%(详见方法)。随着TTA-Nd-NPs自然冷却恢复到室温时, TTA-UCL强度的持续下降趋势,而具有恒定温度的对照组的TTA-UCL强度始终保持不变。(补充图10)。此外,通过调节敏化剂的浓度比,可以容易地控制TTA-UCL的热敏感性(补充图11)。清楚地观察到TTA-UCL强度与635 nm激发功率密度之间的二次-线性相关性,并且阈值激发强度显示为65mWcm-2(图3a)。在低于阈值的低功率激发下,激活剂的三线态自发湮灭导致二次相关,这是双组分TTA上转换系统中的常见现象。此外,TTA-Nd-NPs中Nd3 纳米荧光粉的发光强度与808 nm激发功率密度呈线性关系(图3a),绝对量子效率为10.2%(详见方法)。
在以下实验中,耦合的635和808 nm激发光的功率密度因此被设置为超过阈值(gt;65 mWcm-2)以确保两个发光过程处于线性状态。在此,100-200 mWcmminus;2范围内的激光功率密度是激发的最佳选择,可以在低功率区域中实现与功率无关的信号输出(图3a)。通过对TTA体系的所有上述升级,理论上解决了不规则(或不敏感)温度响应和浓度依赖性的问题,构建了基于TTA体系的比率探针的概念。
TTA-Nd-NPs的比率响应。然后,我们对TTA-Nd-NPs的热敏性质进行了准确研究。如图3b所示,在双通道测试系统中测量TTA-Nd-NPs的发光光谱。在测量过程中,样品温度被精确控制(plusmn;0.1 K),将热电偶放置在样品溶液中,而不是放在试管表面周围(补充图12)。随着温度的升高,TTA-UCL强度迅速增强,呈现出二次趋势(图3c)。在10–50°C(补充图13)范围内,TTA-UCL在TTA-Nd-NPs(约12% K-1)中的计算热灵敏度远高于报告的热灵敏度NaYF4:Yb,Er@NaLuF4 UCNPs(约0.8% K-1)。相比之下,TTA-Nd-NPs中Nd3 纳米晶体的发射缓慢下降,斜率小于0.03% K-1(图3c)。实际上,Nd3 由于其低热灵敏度而不利于热响应。由于作为温度响应单元的TTA体系具有高度的热敏性,因此可以将热不敏感的Nd3 纳米晶体设计为仅作为内部标准。Nd3 纳米晶体的吸收/发射显示与TTA体系的吸收/发射没有重叠,这使得TTA体系的性能不受影响。事实上,TTA体系的校准单元也可以在未来进行升级,例如采用其他基于稀土离子的核壳纳米粒子,这些纳米粒子显示出明显的热敏感性,这可能有利于在比率测温中获得更好的性能。
在生物系统中,外源探针的发光通常取决于特定的生物分布(补充图14)。在此,适当地使用比率纳米胶囊策略来解决这一问题。对于每个单独的TTA-Nd-NPs胶囊,理论上TTA二元体和Nd3 纳米晶体的发光比保持相同,确保了与浓度无关的输出。校准TTA-UCL信号输出(ITTA-UCL/IReference的比)不随初始材料(15 mg mL-1)到极稀溶液(0.9 mg mL-1)的浓度变化而变化,即使TTA-UCL信号大大减少,显示出明显的浓度依赖性信号输出(图3d)。观察结果清楚地证明了比率探测方法对TTA体系的重要性。此外,还研究了在不同情况和组织中变化的pH因子,并且在5.0-8.0的pH下的结果几乎是均匀的(补充图15)。此外,TTA-Nd-NPs探针稳定且具有良好的可逆性(补充图16)。这些性质使得TTA-Nd-NPs适合体内温度成像而不受生物环境的干扰。
基于TTA-Nd-NPs的体内比率测温法。用于体内实际温度评估的TTA-Nd-NPs的标准曲线在生物成像系统中校准(图4a)。组织模型中的模拟条件类似于体内皮下注射(补充图17),数据点拟合为下式:R2gt;0.999,比率(ITTA-UCL/IReference)=0.00375T2-2.12032T 300.47099(图4b)。然后在活体小鼠的温度测定中验证该校准曲线的适用性(补充图18)。实际上,TTA-Nd-NPs可以在没有物理接触的情况下原位显示皮下温度,这优于需要皮肤穿刺的传统热电偶。因此,热灵敏度曲线[SR=(dRatio/dT)/Ratio]如补充图所示。基于这些结果,热敏感度达到约7.1% K-1,分辨率高达约0.1 K,这是迄今为止为活体内温度测量开发的所有温度探针中最佳结果(补充表1)。坦率地说,这种优秀的TTA-Nd-NPs温度探针的弱点为绿色UCL信号的中等穿透深度(补充图20)。因此,在近红外领域工作的热敏TTA-UC系统可能是未来深部组织应用的一个有吸引力的突破。作为参考的近红外辐射敏化剂也可以简化系统的结构。
图4 体内比率测温。体内比率测温设置的示意图。b用组织体模中的TTA-Nd-NPs探针测量体内温度评估的标准曲线。 c基于TTA-Nd-NPs在炎症模式下的比率测温。 明亮的图像显示在用卡拉胶(1 wt%,100 mu;L)刺激的昆明小鼠肿胀的右腿中的关节炎,而左腿是正常的对照。 比例图像显示了两条腿的发光比和评估的温度分布。 TTA-UCL和参考信号分别在体内成像系统的通道I(485-575 nm)和通道II(980-1300 nm)中获得。
此外,我们探讨了我们的体温计在体内的可能应用。通常,炎症与生物系统中的生理紊乱相关,这可能导致与温度相关的变化。炎症现象已经在不同的
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[446332],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 基于环氧树脂的超疏水结构防腐涂层外文翻译资料
- 田口优化技术在确定薄壳类零件注塑成型工艺参数中的应用外文翻译资料
- 形状和尺寸控制的钼酸钙甜甜圈形微结构的合成外文翻译资料
- 纳米多孔钴基ZIF-67金属有机骨架(MOF)在构建具有优异防腐性能的环氧复合涂层中的应用外文翻译资料
- 田口方法在塑料注射模具设计中减少翘曲的应用外文翻译资料
- 浸渍和封装轻质骨料用于自修复混凝土的研究外文翻译资料
- 具有形状恢复和超吸收特性的化学交联纤维素纳米晶体气凝胶外文翻译资料
- 一锅法合成非贵金属WS2/g-C3N4增强型光催化剂制氢外文翻译资料
- 由MOF-74 (Zn)制备具有超快吸附污染物能力和超电 容特性的多功能多孔Zn0-C复合材料外文翻译资料
- 氢键控制的柔性共价有机骨架的结晶度和吸附 性能的机理研究外文翻译资料


